W obliczu niegasnącej pandemii i dostępnej szczepionki przeciwko COVID-19 zagadnienia dotyczące odpowiedzi immunologicznej na SARS-CoV-2 pozostają szczególnie aktualne. Badania nad reakcją układu immunologicznego na SARS-CoV-2 mają kluczowe znaczenie dla postępu prac związanych zarówno z leczeniem COVID-19, jak i oceną skuteczności szczepień ochronnych. Testy laboratoryjne umożliwiające monitorowanie odpowiedzi immunologicznej są obecnie niezwykle cennym narzędziem diagnostycznym.
Rodzaje testów laboratoryjnych służących do oceny odpowiedzi immunologicznej na SARS-CoV-2
Odpowiedź immunologiczna zbudowana jest z dwóch filarów, czyli odpowiedzi humoralnej, za którą odpowiadają limfocyty B i przeciwciała, oraz odpowiedzi komórkowej, w której uczestniczą limfocyty T, a dokładnie limfocyty T pomocnicze oraz limfocyty T cytotoksyczne.
Testy służące do pomiaru poziomu specyficznych przeciwciał anty-SARS-CoV-2, które zostały wytworzone w odpowiedzi na zakażenie lub podaną szczepionkę, są powszechne i łatwo dostępne. Korzystne jest, jeżeli w przypadku monitorowania humoralnej odpowiedzi immunologicznej wykorzystamy ilościowe testy pozwalające precyzyjnie określić poziom przeciwciał o właściwościach neutralizujących, czyli przeciwko antygenowi S1 wirusa SARS-CoV-2. Przykładem takiego narzędzia jest test Anty-SARS-CoV-2 QuantiVac ELISA (IgG). Czy badanie przeciwciał jest jedynym narzędziem, którym w tym momencie dysponujemy? W badaniach oceniających odpowiedź immunologiczną (np. poszczepienną) istotną rolę odgrywają również testy umożliwiające ocenę odpowiedzi komórkowej.
EUROIMMUN Quan-T-Cell SARS-CoV-2
Firma EUROIMMUN wprowadziła nowy test do oceny komórkowej odpowiedzi immunologicznej przeciwko SARS-CoV-2: Quan-T-Cell SARS-CoV-2 (IGRA, Interferon-Gamma Release Assay). Testy typu IGRA służą do określenia aktywności komórek T reagujących na patogen poprzez wykrywanie interferonu gamma (IFN-γ), ważnej cząsteczki sygnałowej układu immunologicznego. Na czym dokładnie polega działanie testu IGRA?
Zasada działania testu Quan-T-Cell SARS-CoV-2 (IGRA)
Materiałem do badania jest świeżo pobrana krew pełna (jako antykoagulant wykorzystuje się heparynę). We krwi pacjenta, który miał kontakt z wirusem SARS-CoV-2, obecne są limfocyty T zdolne do rozpoznawania antygenów tego patogenu. Proces ten wiąże się z syntezą i uwalnianiem IFN-γ. Wykrywanie i ilościowe oznaczenie IFN-γ wydzielonego po pobudzeniu w warunkach in vitro limfocytów T stanowi istotę testu IGRA. W przypadku testu EUROIMMUN Quan-T-Cell SARS-CoV-2 oznaczenie dzieli się na 2 etapy:
- pobudzenie w warunkach in vitro limfocytów T antygenem specyficznym dla SARS-CoV-2, tj. podjednostką S1 białka S SARS-CoV-2
- ilościowa ocena wydzielonego przez limfocyty T IFN-γ za pomocą testu ELISA
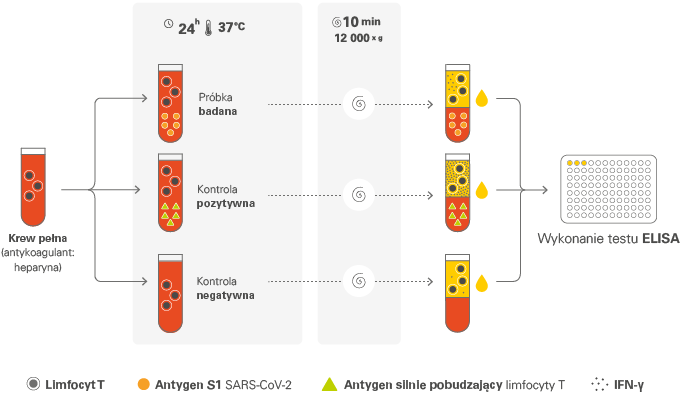
Rys. 1. Zasada działania testu EUROIMMUN Quan-T-Cell SARS-CoV-2.
W pierwszym etapie świeżo pobrana krew pełna inkubowana jest z antygenem S1 wirusa SARS-CoV-2 opłaszczonym na dnie probówki testowej. Jeśli limfocyty T miały wcześniejszy kontakt z antygenami wirusa SARS-CoV-2 w organizmie pacjenta, na skutek ich pobudzenia przez antygen S1 w warunkach in vitro dochodzi do wydzielania IFN-γ. Krew pełna jest również inkubowana w drugiej probówce z kontrolą ujemną (ocena nieswoistej odpowiedzi tła) oraz w trzeciej probówce z kontrolą dodatnią (ocena ogólnej odpowiedzi limfocytów T po stymulacji). Do zalet zestawu do stymulacji limfocytów T testu Quan-T-Cell SARS-CoV-2 zalicza się między innymi brak konieczności izolacji jednojądrzastych komórek krwi obwodowej (PBMC).
W drugim etapie wykonuje się test ELISA umożliwiający pomiar wydzielonego IFN-γ w pierwszym etapie testu. W wyniku przeprowadzonej analizy otrzymuje się wynik ilościowy. Drugi etap testu IGRA, czyli oznaczenie poziomu IFN-γ metodą ELISA, można w pełni zautomatyzować za pomocą dostępnych systemów EUROIMMUN (Analyzer I, Analyzer II-P, EUROLabWorkStation). Dodatkowo oprogramowanie EUROLab Quan-T-Cell wspiera automatyczny odczyt wyników.
Kompleksowe badania odpowiedzi immunologicznej
Dostępne dane literaturowe sugerują, że oba filary układu immunologicznego, odpowiedź specyficznych przeciwciał i limfocytów T, są ważne dla zrozumienia odporności na reinfekcję SARS-CoV-2. Najprawdopodobniej około 10% pacjentów, którzy odczuwali objawy COVID-19, i 40% pacjentów, którzy przeszli chorobę asymptomatycznie, traci przeciwciała IgG w stosunkowo krótkim czasie (1). W tym wypadku przebyte zakażenie można wykryć jedynie poprzez pomiar komórkowej odpowiedzi immunologicznej. Ponadto uważa się, że aktywność limfocytów T jest związana z silną ochroną immunologiczną, nawet przy braku detekcji przeciwciał przeciwko SARS-CoV-2.
Pomimo prowadzonych od ponad roku intensywnych badań naukowych w dziedzinie infekcji SARS-CoV-2 nadal jest wiele niewiadomych. Jak mówi dr Wolfgang Schlumberger (2), Dyrektor Generalny EUROIMMUN: „Wiele pytań dotyczących postępu choroby COVID-19 i rozwoju długotrwałej odporności po zakażeniu lub szczepieniu wciąż pozostaje bez odpowiedzi. Oba testy, SARS-CoV-2 IGRA oraz ELISA Anty-SARS-CoV-2 QuantiVac, umożliwiają badaczom znacznie dokładniejsze i szersze badanie odpowiedzi immunologicznej na nowego koronawirusa, a co za tym idzie – przybliżają nas do poznania odpowiedzi na postawione pytania”.
W badaniach nad potencjalną odpornością na SARS-CoV-2 istotne jest kompleksowe podejście do oceny odpowiedzi układu immunologicznego: zarówno humoralnej, jak i komórkowej. Testy laboratoryjne umożliwiające określenie poziomu przeciwciał anty-SARS-CoV-2, a także zbadanie reaktywności limfocytów T, są obecnie niezwykle cennym narzędziem diagnostycznym, ułatwiającym zrozumienie skomplikowanych mechanizmów immunologicznych w przebiegu COVID-19.
Piśmiennictwo
- Tan Wenting et al., Viral kinetics and antibody responses in patients with COVID-19, MedRxiv (2020).
- Wu Fan et al., Neutralizing antibody responses to SARS-CoV-2 in a COVID-19 recovered patient cohort and their implications, MedRxiv (2020).

Katarzyna Buska-Mach
Kierownik Działu Promocji Produktów i Szkoleń Stacjonarnych, Senior Product Manager ds. Neurologii i TORCH 10






Dodaj komentarz